
2024年,国家药监局创新特别审查程序(简称“创新审批”)公示的第三类医疗器械共计69件,其中IVD产品3件。与2023年的2件相比,IVD产品获批数量增长稳健。2024年优先审查程序公示(简称“优先审批”)的第三类医疗器械共计20件,其中IVD产品9件。与2023年4件相比,IVD产品增量显著。创新医疗器械特别审查程序是为了鼓励医械的研究与创新、促进新技术的推广和应用的特殊审批通道。2024年,有69件第三类医疗器械产品进入到创新审批程序,其中有3家企业的3件IVD产品。表1.2024年进入国家药监局创新审批程序IVD产品
与2023年相比,创新医疗器械审批总量增长微弱,仅增长2件,其中IVD产品则增长也只有1件,从2023年的2件增长到3件,这与创新审批程序标准高、审查严是一致的。2024年,国家药监局优先审批程序共公示了20件第三类医疗器械,其中有9件IVD产品,包括试剂7件、仪器2件。
表2.2024年进入国家药监局优先审批程序IVD产品
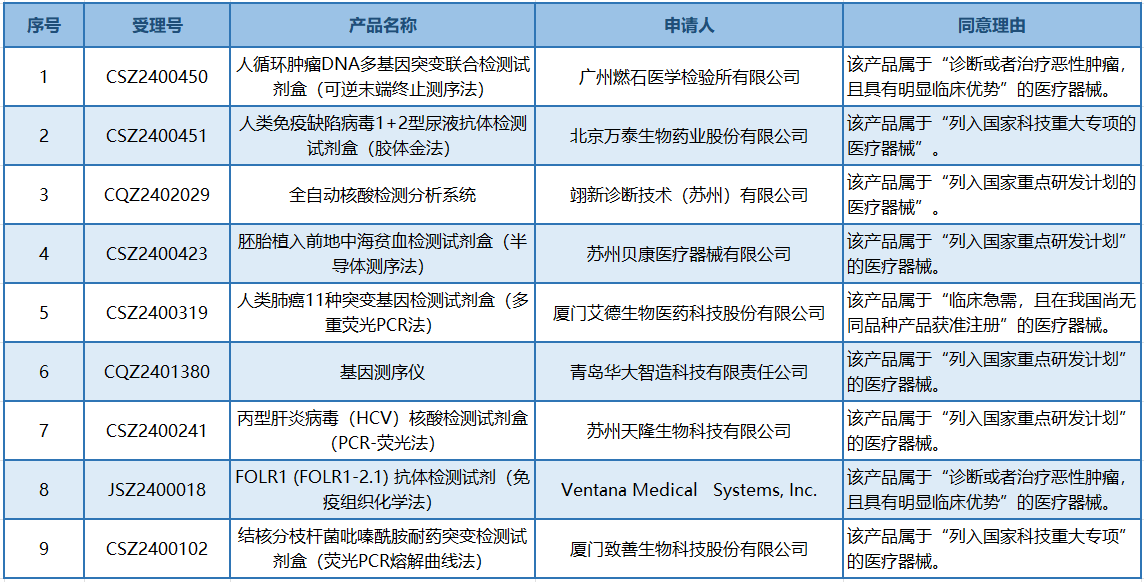
优先审批针对的产品有五大类:一是诊断或治疗罕见病、恶性肿瘤且具有明显临床优势的医疗器械;二是诊断或治疗老年人特有和多发疾病且尚无有效诊断或治疗手段的医疗器械;三是专用于儿童且具有明显临床优势的医疗器械;四是列入国家科技重大专项或国家重点研发计划的医疗器械;此外还有一个“其他情形”。9件进入优先审批的IVD产品,“同意理由”中,属于“列入国家科技重大专项或国家重点研发计划的”6件,属于“临床急需,且在我国尚无同品种产品获准注册”的1件,属于“诊断或者治疗恶性肿瘤,且具有明显临床优势”的2件。与2023年同期相比,医疗器械优先审批呈现了增长态势,总量达到1.5倍的增长,IVD产品增长率也超过一倍。创新审批和优先审批都是医疗器械审批的特别程序,从近两年的审批情况看,总量呈现出了稳步增长的态势,特别是IVD产品的优先审批。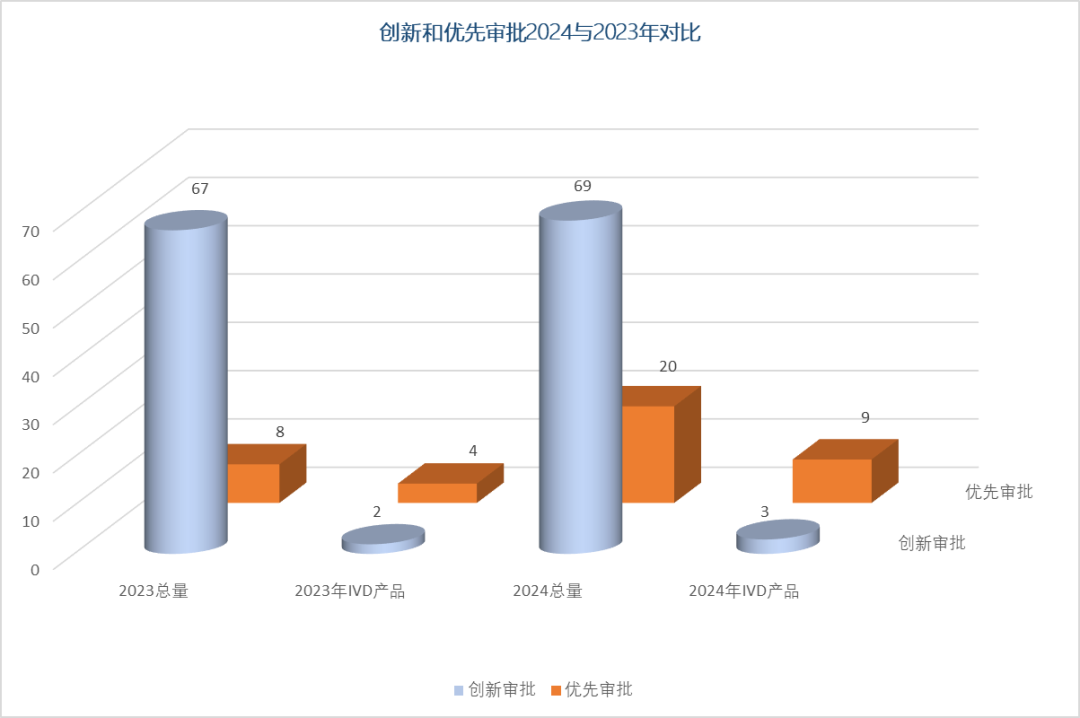
国家药监局对第三类医疗器械进行创新和优先审批,各省级药监部则对本辖区范围内的第二类医疗器械进行创新和优先审批。从2024年已经发布创新和优先审批结果的省市自治区看,IVD产品也呈现出分布不均、差异明显的状况。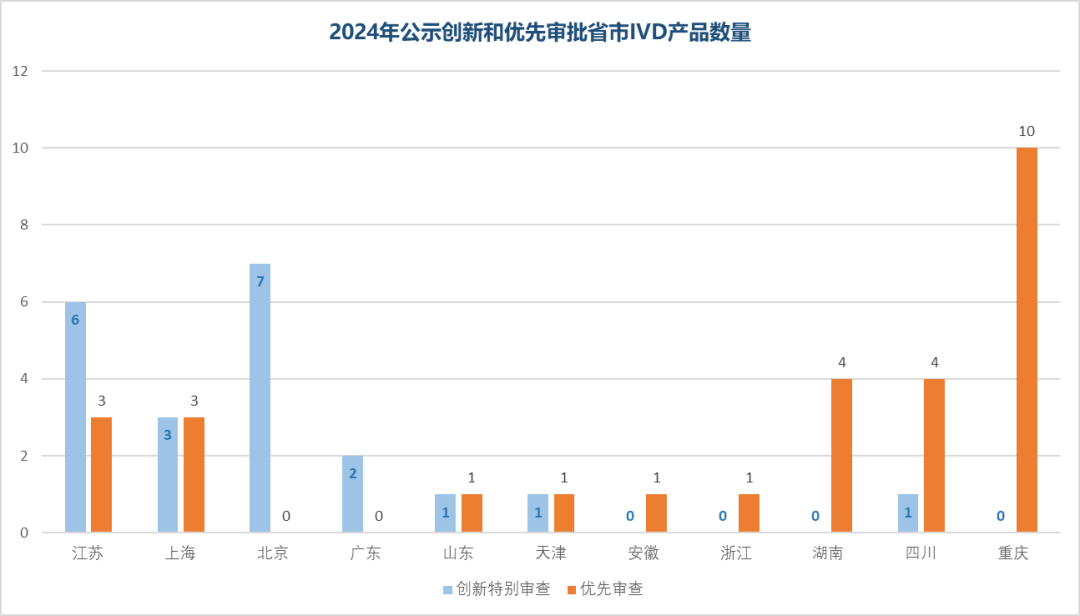
2024年IVD创新和优先审批中,厦门艾德生物医药科技股份有限公司表现亮眼——创新、优先审批均有上榜!本年度的普通程序之中,“艾德生物”也有三件试剂和一件仪器获批。“艾德生物”于2017年在创业板上市,是肿瘤精准医疗伴随诊断的标志性IVD企业。2024年前三季度,“艾德生物”以1.46亿元研发总投入,居中国IVD企业研发投入榜单第11名;在研发/营收比榜单上进入十强,排名第六。
三类医疗器械的创新优先审批,标准高、审查严。能够进入程序的,前者需要“国内首创”且“国际领先”;后者除了产品技术创新之外,还需要深度解读产业政策,把握国家战略和预判产业趋势。2024年进入的创新优先审批的这些项目,为关注这两个通道的企业,提供了参考样板。
2024年9月13日,国家药监局局长李利表示,将加快临床急需创新药和医疗器械的审评审批,将符合条件的产品纳入优先审评审批程序,缩短技术审评、注册核查、注册检验等各环节时限,加快审批步伐。在国家政策的加持、产学研转化机制的成功落地、以及企业在研发上的大力投入等多重力量的共同推动之下,预计2025年,将会有更多IVD项目进入创新优先审批通道。















发表评论 取消回复