一周热点资讯
01 事件:
奥泰生物年产4亿人份体外诊断试剂生产研发中心建设项目延期
西门子医疗全自动生化免疫分析仪在上海研发与生产基地正式投产
《糖化血红蛋白即时检测临床应用专家共识(2025)》发布
亚辉龙捐赠781万元物资,助力河源和平县乡村振兴事业
02 政策:
国家卫健委、国家中医药局、国家疾控局联合发布了《关于进一步加强医疗机构电子病历信息使用管理的通知》
国家药监局发布《国家药监局关于发布优化全生命周期监管支持高端医疗器械创新发展有关举措的公告》
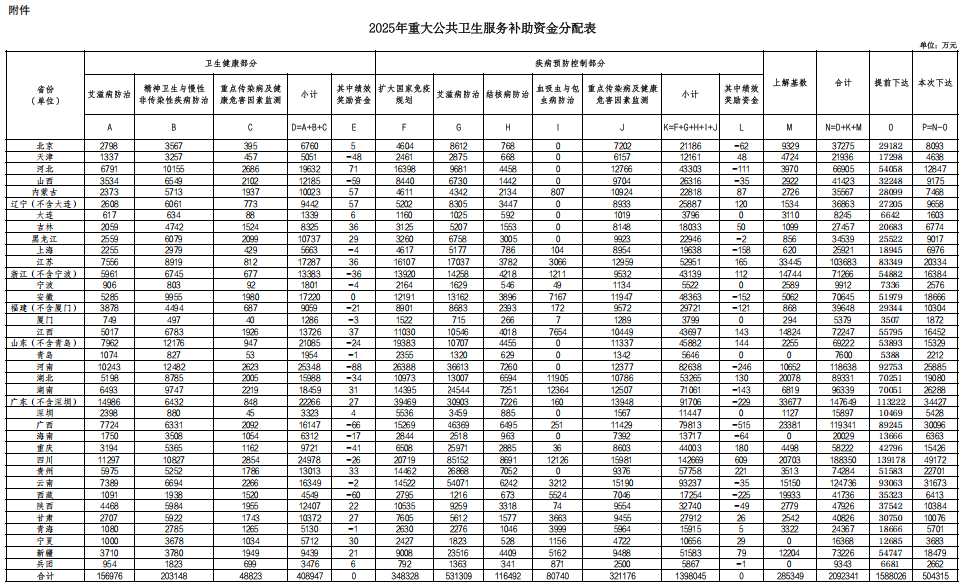
三部门联合发布《关于下达2025年重大公共卫生服务补助资金预算的通知》
为进一步支持我国医疗器械产品出口贸易,规范出口销售证明办理服务,国家药品监督管理局组织起草了《医疗器械出口销售证明管理规定(修订草案征求意见稿)》
03 新产品/技术:
04 战略合作:
1、奥泰生物年产4亿人份体外诊断试剂生产研发中心建设项目延期
7月1日,奥泰生物发布公告,将“杭州奥恺生物技术有限公司年产4亿人份体外诊断试剂生产研发中心建设项目”的预期达到可使用状态日期从2025年6月延期至2025年12月。此次延期主要受到外部宏观环境、装修进度及研发项目进度等多方面因素的影响。2、西门子医疗全自动生化免疫分析仪在上海研发与生产基地正式投产西门子医疗的首款国产高端实验室诊断设备——Atellica全自动生化免疫分析仪,在上海研发与生产基地正式投产,标志着西门子医疗实现了大型影像诊断设备、临床介入治疗设备以及实验室诊断设备的全线国产。该设备以其卓越性能和自动化水平,助力国内顶尖医疗机构优化流程、提升运营效率。其国产化不仅全面传承了全球品质标准,还通过自动质控、视觉识别等前沿技术,实现了质量与效率的双重提升。3、《糖化血红蛋白即时检测临床应用专家共识(2025)》发布
6月28日发布的《糖化血红蛋白即时检测临床应用专家共识(2025)》指出,即时检测(POCT)技术为糖化血红蛋白(HbA1c)检测提供了新途径,具有操作简便、快速出结果的特点,显著提升了糖尿病管理的可行性和效率。其核心价值包括:初诊筛查中识别糖尿病高危人群,缩短诊断-干预时间窗;复诊随访中实时评估治疗效果,为调整降糖方案提供依据;急诊或围术期等特殊场景下结合血糖监测判断长期代谢控制水平,指导急性期管理决策。POCT支持的频繁监测可灵敏捕捉血糖波动趋势,避免因检测延迟导致的控制恶化。其设备的小型化与便携性使其可延伸至社区筛查、家庭医生签约服务等场景,对我国基层糖尿病防控具有战略意义。
4、亚辉龙捐赠781万元物资,助力河源和平县乡村振兴事业
深圳市亚辉龙生物科技股份有限公司在广东省“6·30”助力乡村振兴活动日之际,奔赴河源市和平县启动“助学援校赠医”慈善项目。亚辉龙向和平县捐赠了价值781.25万元的物资,实施“困境儿童教育援助”“山区学校体育健康支援”“医疗检测水平提升”三大计划,以改善当地教育环境和提升医疗服务水平。此次捐赠是亚辉龙履行社会责任、响应国家乡村振兴战略的重要举措,旨在助力和平县教育与医疗事业的发展,为困境中的孩子们带来美好的未来。1、国家卫健委、国家中医药局、国家疾控局联合发布了《关于进一步加强医疗机构电子病历信息使用管理的通知》6月30日,国家卫健委、国家中医药局、国家疾控局联合发布《关于进一步加强医疗机构电子病历信息使用管理的通知》,对电子病历的内部管理、使用规范、数据安全、监管落实提出更高要求,推动医疗数字化、智能化、标准化发展。电子病历作为医疗数据的核心载体,其广泛应用将加速检验结果互认机制及设备数据互联互通。对IVD行业而言,需提升产品质量和结果一致性,以适应检验结果互认带来的新要求;同时,设备数智化水平也需提高,以满足与医院信息系统的无缝对接。国产IVD企业面临新机遇与挑战,需主动适配,加快设备数智化升级,深化合作,提供高质量检验产品和数据闭环解决方案。2、国家药监局发布《国家药监局关于发布优化全生命周期监管支持高端医疗器械创新发展有关举措的公告》7月3日,国家药监局发布《国家药监局关于发布优化全生命周期监管支持高端医疗器械创新发展有关举措的公告(2025年第63号)》。聚焦医用机器人、高端医学影像、人工智能医疗器械、新型生物材料等前沿领域,推动医疗器械迈向更高质量、更高技术、更强监管的新阶段。《公告》明确提出优化高端医疗器械的全生命周期监管,重点支持关键领域的创新发展,实施创新特别审查程序,简化核心算法不变而性能优化产品的变更注册要求等。同时,强化上市后质量安全监测,重点关注高端有源医疗器械的使用期限、临床维护及不良事件主动监测机制。3、三部门联合发布《关于下达2025年重大公共卫生服务补助资金预算的通知》7月2日,财政部、国家卫生健康委、国家疾控局联合发布《关于下达2025年重大公共卫生服务补助资金预算的通知》,补助资金合计约209.23亿元,重点支持艾滋病、结核病、重点传染病、慢性病防控等领域。这将推动IVD检测产品需求增长,尤其是疾病筛查、重点传染病监测、免疫规划等方面。4、国家药品监督管理局组织起草了《医疗器械出口销售证明管理规定(修订草案征求意见稿)》7月2日,国家药监局发布《医疗器械出口销售证明管理规定(修订草案征求意见稿)》,向社会公开征求意见,意见反馈截止日期为2025年8月2日。此次修订旨在落实国务院办公厅要求,进一步支持我国医疗器械产品出口贸易,规范出口销售证明办理服务,通过制度优化畅通出口渠道,降低企业制度性交易成本,鼓励电子化办理以提升政务服务效能。李敏教授与汪骅教授团队在《Advanced Science》发表封面论文,开发了名为CasμChip的微流控芯片平台,可同步、快速、数字化检测结直肠癌相关环状RNA(circRNA)生物标志物circCK1γ3和circWDR37,为结直肠癌的无创早期筛查提供了新技术支持。该平台融合CRISPR诊断与微流控液滴技术,解决了多重circRNA检测中的定量和正交性难题,具有快速报告、精准定量等优势,在基层医疗机构等具有广阔应用前景。研究发现两者联合检测可将CRC筛查的曲线下面积提升至0.808,优于单一标志物及传统肿瘤标志物。赛默飞世尔科技的Oncomine Dx Express检测获得美国FDA批准,作为Dizal的Zegfrovy的伴随诊断和肿瘤分析。该检测用于识别携带EGFR外显子20插入突变的非小细胞肺癌患者,以确定其是否适合接受Zegfrovy治疗。Zegfrovy成为唯一针对这些EGFR突变的NSCLC的靶向口服治疗药物。Oncomine Dx Express检测可在24小时内生成结果,支持及时的治疗决策。3、东南大学和基蛋生物合作开发了一种基于RPA恒温核酸扩增技术的手持式分子POCT系统近日,东南大学和基蛋生物合作开发了一种基于RPA恒温核酸扩增技术的手持式分子POCT系统,能在25分钟内检测8种呼吸道病原体,包括甲型/乙型流感病毒、呼吸道合胞病毒等。该系统采用微流控技术,通过创新的气压驱动流体泵送策略实现样本裂解、核酸释放与扩增的一体化。其设计降低了检测成本,单次检测低于1.4美元,且操作简便,结果可通过蓝牙或HTTP协议推送至手机。经过验证,该系统灵敏度超97%,特异性超99%,适用于居家自测、社区医疗和资源有限地区,为呼吸道疾病的快速、低成本检测提供了新方案。6月30日,复星诊断与西门子医疗宣布达成战略合作,推出首个联合新品国产生化试剂解决方案。该方案基于西门子医疗国产Atellica检测平台,由复星诊断完成本土化研发与生产,覆盖多个领域,已获16个试剂及其对应校准品的注册证,预计下半年上市。此次合作将整合技术、产能与全球化资源,推动体外诊断领域创新升级,降低终端用户成本,缩短产品交付周期,提升用户体验,助力医疗机构降本增效,为后续联合开发及全球化合作奠定基础。7月2日,万孚生物与上海金标生物科技有限公司正式签署全球本地化生产战略合作协议。双方将整合生物技术、制造技术及智能制造等优势,为国际合作伙伴提供快速诊断试剂生产及销售的一站式服务。这是万孚生物深化全球战略布局、拓展海外本地化能力的重要举措,旨在助力区域医疗健康产业协同发展,携手守护全球健康。通过此次合作,双方将加速本地化生产项目落地,降低区域市场对进口诊断试剂的依赖,提升公共卫生可及性。














发表评论 取消回复